من اهل الدار
الياسري
تاريخ التسجيل: September-2013
الدولة: العراق العظيم
الجنس: ذكر
المشاركات: 11,553 المواضيع: 1,428
صوتيات:
43
سوالف عراقية:
0
مزاجي: برتقالي
المهنة: مدرس
أكلتي المفضلة: دولمة
موبايلي: Samsung A55
آخر نشاط: منذ 2 ساعات
الاتصال:
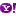
طفرة هرمونية بعد الولادة قد تفسّر بداية مرض كينيدي النادر لدى الرجال
كشف باحثون أن الارتفاع الطبيعي في هرمون التستوستيرون مباشرة بعد الولادة قد يشكّل اللحظة الحاسمة لانطلاق مرض وراثي نادر يؤثر على الأعصاب لدى الذكور.
صورة تعبيرية / Gettyimages.ru
وقد يفتح هذا الاكتشاف آفاقاً جديدة لتطوير تدخلات علاجية مبكرة يمكن أن تغيّر مسار المرض بشكل جذري. ويُعرف هذا المرض باسم ضمور العضلات الشوكي البصلي (SBMA) أو مرض كينيدي، وهو اضطراب وراثي نادر يصيب الرجال، ويتسبب بضعف تدريجي وهزال في العضلات.
عادةً ما تبدأ العلامات الأولى للمرض، مثل رعاش اليد، في الظهور خلال الثلاثينيات من العمر، إلا أن التشخيص يتأخر غالباً حتى الأربعينيات، عندما يصبح ضعف العضلات أكثر وضوحاً. وبما أن المرض يرتبط بارتفاع هرمون التستوستيرون، فهو يقتصر على الذكور.
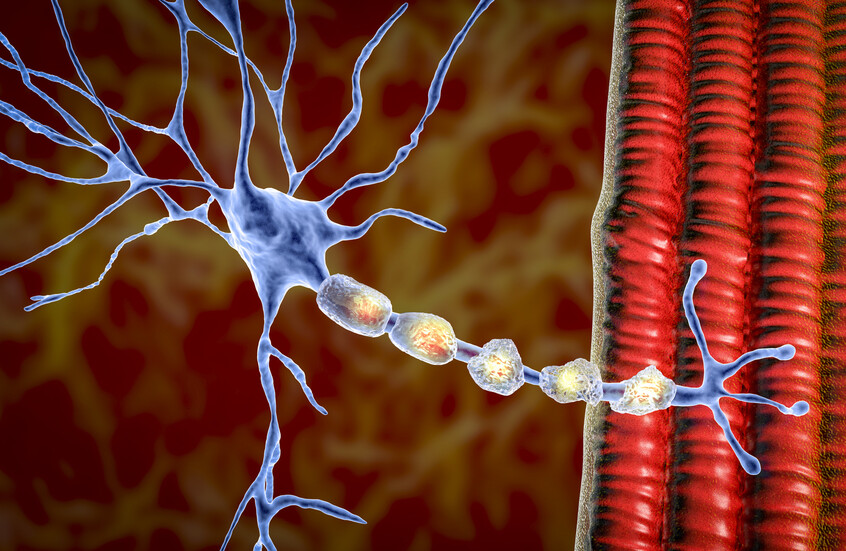
طفرة هرمونية مبكرة وتأثيرها على الأعصاب
توصل فريق بحثي في جامعة ناغويا اليابانية إلى أن الارتفاع الطبيعي في التستوستيرون بعد الولادة يؤدي إلى تنشيط مفرط للخلايا العصبية الحركية لدى الفئران التي تحمل الطفرة الجينية المرتبطة بالمرض. هذا النشاط الزائد يستمر بشكل ضار، وينتهي بتلف تلك الخلايا عند بلوغ مرحلة النضج.
وقد أظهرت نتائج الدراسة، المنشورة في مجلة Nature Communications، أن التدخل العلاجي المبكر عند الولادة ساهم بشكل كبير في تقليل هذا التلف.
ورغم أن تراكم البروتينات غير الطبيعية في أمراض التنكس العصبي يبدأ قبل ظهور الأعراض بسنوات طويلة، فإن ما يحدث خلال هذه المرحلة المبكرة لا يزال غير واضح بشكل كامل. لذلك ركّزت هذه الدراسة على الأيام الأولى من الحياة باعتبارها مرحلة مفصلية.
"البلوغ المصغر" ودوره في بدء المرض
يحدث لدى جميع ذكور الثدييات ارتفاع مؤقت في هرمون التستوستيرون بعد الولادة، يُعرف باسم "طفرة التستوستيرون الحديثي الولادة" أو "البلوغ المصغر". يستمر هذا الارتفاع لنحو 10 أيام لدى الفئران، ويصل إلى حوالي 6 أشهر لدى البشر.
وبما أن البروتين المتحوّر المسؤول عن المرض يحتاج إلى التستوستيرون للدخول إلى نواة الخلايا العصبية والتسبب في الضرر، افترض الباحثون أن هذه المرحلة تمثل نقطة البداية المبكرة للمرض.
وأوضح الباحث توموكي هيروناغي أن البروتين المعيب يبدأ بالتراكم داخل نوى الخلايا العصبية الحركية منذ اليوم الأول بعد الولادة لدى الذكور المصابين، نتيجة هذا الارتفاع الهرموني. في المقابل، لم تظهر الإناث التي تحمل نفس الطفرة هذه التأثيرات، مما يؤكد الدور المحوري للتستوستيرون.
نشاط عصبي غير طبيعي منذ الأيام الأولى
أظهرت الدراسة أيضاً أن الجينات المرتبطة بتنشيط الخلايا العصبية، وخاصة مستقبلات الغلوتامات، تكون في حالة نشاط مفرط خلال الأسبوع الأول من الحياة لدى الفئران المصابة، ما يؤدي إلى فرط نشاط الخلايا العصبية الحركية.
والمثير للاهتمام أن هذا النمط نفسه لوحظ في خلايا عصبية نُميت مخبرياً من مرضى بشريين، ما يشير إلى أن آلية المرض لدى الإنسان قد تكون مماثلة لما تم رصده في النماذج الحيوانية.
أمل جديد: العلاج المبكر يغير النتائج
لاختبار إمكانية العلاج المبكر، استخدم الباحثون نوعين من الأدوية على فئران حديثة الولادة:
- العلاج الأول: استهدف البروتين المعيب مباشرة، ما أدى إلى تقليل مستوياته بشكل مؤقت.
- العلاج الثاني: استهدف بروتين REST4، الذي يلعب دوراً رئيسياً في فرط النشاط العصبي، وساهم في إعادة التوازن للنشاط الجيني داخل الخلايا العصبية.
وقد أظهر كلا العلاجين نتائج إيجابية، حيث حسّنا البقاء على قيد الحياة والأداء الحركي، وقللا من تدهور الخلايا العصبية عند تقييم الفئران بعد 13 أسبوعاً.
وأشار هيروناغي إلى أن من أكثر النتائج إثارة أن إعطاء العلاج عند الولادة وفّر حماية طويلة الأمد للخلايا العصبية، رغم أن تأثير الدواء استمر لفترة قصيرة فقط، ما يدل على أن التدخل في التوقيت المناسب قد يُحدث فرقاً دائماً.
آفاق مستقبلية واعدة
يُعد بروتين REST4 هدفاً جديداً واعداً لتطوير علاجات مستقبلية. وكانت جامعة ناغويا قد طوّرت سابقاً دواء ليوبروريلين أسيتات، وهو العلاج الوحيد المعتمد في اليابان لهذا المرض، ما يعزز أهمية هذه النتائج ضمن سياق بحثي مستمر.
ويعمل الفريق حالياً على التحقق مما إذا كانت نفس التغيرات العصبية تحدث لدى المرضى البشر، إضافة إلى تقييم سلامة وفعالية العلاجات الجينية، تمهيداً لنقل هذه النتائج من المختبر إلى التطبيق السريري.
نقلا عن ميديكال إكسبريس






 رد مع اقتباس
رد مع اقتباس